改訂新版 世界大百科事典 「ホウ(硼)酸」の意味・わかりやすい解説
ホウ(硼)酸 (ほうさん)
boric acid
ホウ素のオキソ酸の総称で,オルトホウ酸,メタホウ酸,四ホウ酸などがある。
オルトホウ酸
化学式B(OH)3。これを単にホウ酸ということもある。天然にはホウ酸石として火山の噴気口に産し,イタリアのトスカナ地方のものは有名である。ホウ酸塩を硫酸,塩酸等と反応させるとたやすく生じ,また酸化ホウ素を水と反応させても得られる。比重1.48,融点170.9℃。透明な無色の六角片状である。構造は図1に示すように,平面状のBO3団が水素結合でつながった巨大分子である。原子間距離はB-O=1.361Å,O-H=0.88Å,O…H=1.84Åで,2種のO-H結合の長さの違いがかなり大きい。加熱すると100℃でメタホウ酸に変化する。水に対する溶解度5.44重量%(25℃)。溶解度は温度とともに著しく増大する。水溶液中ではきわめて弱い酸で,酸解離定数pKa=5.6×10⁻10(25℃)。しかしマンニット,グリセリン等の多価アルコールを加えると,その水酸基と次に示すようなエステル型陰イオンをつくり,これが強酸である。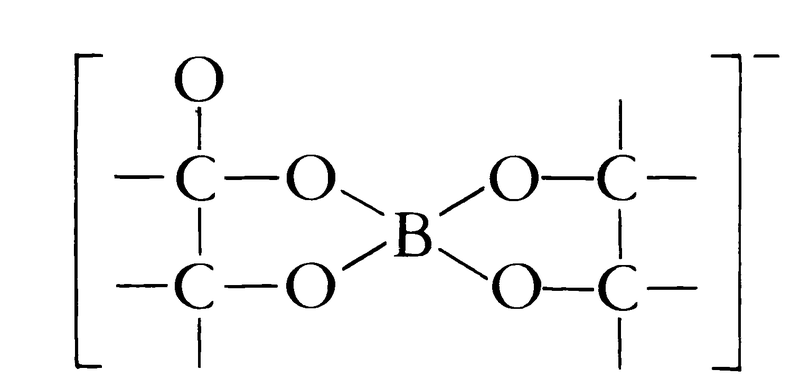
この反応を利用して中和滴定によりホウ酸の定量をすることができる。
メタホウ酸
化学式HBO2。オルトホウ酸を100℃以上に加熱すると脱水して生成する。3種の構造があるが,いずれも水素結合でつながった巨大分子構造である(図2)。表に性質と構造を示す。
四ホウ酸tetraboric acid
化学式H2B4O6。ホウ酸を140℃で40時間加熱すると得られる。このナトリウム塩Na2B4O7・10H2Oをホウ砂という。この陰イオンの構造は,2個の四面体形BO4が酸素1原子を共有し,これらが平面BO3と環をつくり,さらにこの二つの環が融合した形となっている(図3)。したがって化学式はNa2[B4O5(OH)4]・8H2Oと書かれる。
次ホウ酸subboric acid
化学式B2(OH)4。四塩化二ホウ素の加水分解で得られる白色固体。水と反応し水素を発生してオルトホウ酸となる。強い還元性をもつ。
執筆者:水町 邦彦
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報