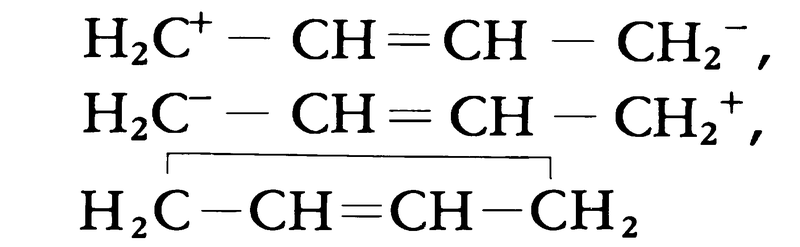共役二重結合 (きょうやくにじゅうけつごう)
conjugated double bond
二つまたはそれ以上の二重結合が単結合と交互に存在する結合をいう。二重結合が孤立して存在する場合とは著しく異なる物理的および化学的性質を示す。共役二重結合をもつ有機物としては,ブタジエンなどのポリエンや,ベンゼンをはじめとする芳香族化合物などがある。ブタジエン分子の化学式はH2C=CH-CH=CH2と記されるが,平面分子で,中央のC-C単結合の長さは,普通の単結合,たとえばエタンの単結合1.54Åより短く,1.48Åである。このことは分子軌道法ではその結合次数が1よりも大きくなることから説明され,共鳴の立場からいえば,
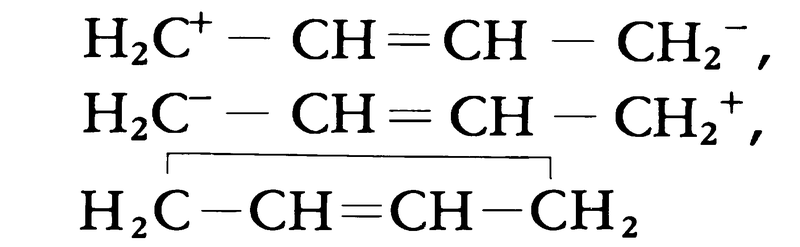
のような構造が多少関与しているとして説明される。また,単結合および二重結合を作る炭素原子の混成の変化も中央の単結合の短縮に寄与している。化学式の示す二重結合がその位置に局在していないことは,いろいろの化学反応にも現れる。たとえばブタジエンに1molの臭素を付加させると,1,2-付加物のほかに1,4-付加物ができる。

1,4-付加反応では二重結合が一つ中央に移動したことがわかる。一般に,多くの共役二重結合をもつ分子は,それと関連した非共役分子に比べて電子吸収スペクトルが長波長側にあり,可視部の光を吸収するので色がついている。たとえばβ-カロチンは11個の共役二重結合をもっていて赤い。ベンゼンのように共役二重結合が環を作った分子では,6個の炭素原子間がまったく平均化されていて,単結合と二重結合の区別がなくなり,分子は正六角形である。
執筆者:佐野 瑞香
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
共役二重結合
きょうやくにじゅうけつごう
conjugated double bond
炭素原子鎖が単結合と二重結合を交互に有するとき,この二重結合を共役二重結合という。最も簡単な例が2個の二重結合をもつ共役ジエン。その二重結合は非共役系化合物と異なった物理化学的性質を示す。いちばん簡単な鎖状共役化合物はブタジエンであり,環状化合物はベンゼンである。ブタジエンに臭素2原子を付加すると,主として1,4付加が起り,少量の1,2付加化合物を生じる。またディールス=アルダー反応の際は1,4付加だけが起る。ベンゼンに低温で臭素を作用させると,非共役系の化合物よりも反応が起りにくい。そのほか酸化還元反応,および水素化熱,燃焼熱の測定から共役二重結合は非共役二重結合と異なった性質をもち,非共役系よりも安定であることが知られている。またブタジエンの中央の炭素-炭素単結合の距離は一般の平均的値 1.54Åに比べて短く 1.46Åである。これらの事実から共役系化合物は古典的ケクレ原子価結合式では満足に表わすことができない。そこでこの性質を説明するのにπ電子の非局在化という考えが導入された。つまり共役二重結合を有する化合物では二重結合のπ電子は特定の炭素原子間に存在するのではなく,分子全体にわたり,炭素-炭素単結合 (σ結合) を含む平面に垂直に分布し,π電子雲の重なりが最大のとき共役系は最も安定となる。ベンゼンの場合も炭素原子間のσ結合から成る正六角形平面の上下にπ電子が分布している。一般に環状共役系のほうが鎖状結合系より安定であり,ベンゼンの各炭素-炭素結合の二重結合性は約 50%,共鳴エネルギーは約 151 j・mol-1 ,ブタジエンでは 20%,共鳴エネルギーは数 j・mol-1 である。共役二重結合の数が増すに従って分子の吸収スペクトルは長波長側に移動する。たとえばジフェニルポリエンの結晶に関する研究では n=1 のとき無色,n=2 のとき微黄色,n=5 のとき橙色である。ニンジンの赤色色素の主成分β-カロテンは CH=CH が 10個の共役二重結合から成る。赤外線吸収スペクトルでは炭素-炭素二重結合の伸縮振動は一般に波数で 1620~1680 cm-1 付近に吸収が出るが,共役二重結合数の多いほど吸収帯の数が増し,かつ低波数側に移動する傾向がある。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
共役二重結合
キョウヤクニジュウケツゴウ
conjugated double bond
2個以上の二重結合がそれぞれ単結合をはさんでつながっているとき,これらの二重結合を共役二重結合という.共役二重結合系が鎖状をなすものの代表としてはブタジエンやポリエンがあり,また環状をなすものとしてはベンゼンやペンタセン,ヘキサセンなどのポリアセンをはじめ芳香族化合物がある.個々の二重結合はσ結合とπ結合とからなり,π結合をつくるπ電子は易動性(非局在性)を有するため,単結合の間でもπ結合を形成することができる.このようにして単結合をはさんだ2個の二重結合は共役することができる.2個の二重結合が共役して単結合の間にπ結合をつくると,両側に孤立したπ電子が残されることになる.これは共役による寄与は鎖状共役系の場合,たとえばブタジエンでは中央の単結合は二重結合性を帯び,1,4-付加体をつくりやすくなるという事実に現れている.また,環状共役系の場合は,単結合と二重結合が交替することによって孤立π電子を残すことなくπ結合が形成される.このため,たとえばベンゼンでは,どの結合も長さが等しく単結合と二重結合の中間の長さになっている.[別用語参照]共鳴
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
共役二重結合
きょうやくにじゅうけつごう
conjugated double bond
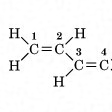
二つ以上の二重結合が一つの単結合を挟んで構成されている結合系をいう。ブタジエンはその代表例であるが、二重結合は1と2、および3と4の間に局在化しているようにみえる(図)。しかし、これらの間に存在するπ(パイ)電子は1から4の炭素の間を流れるので、2と3の間にも二重結合性が生ずる。一般に共役二重結合をもつ分子では、非局在化したπ電子系ができる。環状になった共役結合系の代表はベンゼンで、ケクレが考えたように、6個の炭素が同等に結合しており、二重結合がある炭素間に局在してはいない。石墨(グラファイト)は共役二重結合が平面的に広がっており、したがって良電導体である。
[下沢 隆]
出典 小学館 日本大百科全書(ニッポニカ)日本大百科全書(ニッポニカ)について 情報 | 凡例
百科事典マイペディア
「共役二重結合」の意味・わかりやすい解説
共役二重結合【きょうやくにじゅうけつごう】
単結合と二重結合が交互に連らなった結合をいい,二重結合をつくっている電子がかなり自由に動けるため,実際には単結合と二重結合とが混じり合った中間的な状態になっている。そのため二重結合が孤立して存在する場合とは著しく異なる物理的および化学的性質を示す。共役二重結合をもつ化合物,たとえばブタジエンに臭素2原子を付加させると,臭素原子は両端の炭素原子に結合し新たに中央に二重結合を生ずる。 CH2=CH−CH=CH2+Br2 →CH2Br−CH=CH−CH2Brまた無水マレイン酸などとは環状化合物をつくる芳香族化合物のベンゼン環をつくっている結合も,共役二重結合の例である。→ジエン合成
→関連項目助色団|二重結合
出典 株式会社平凡社百科事典マイペディアについて 情報
共役二重結合
二重結合と単結合が交互に複数連なる構造.二重結合を作るπ電子が隣接する単結合の反対側のπ電子とも弱い結合をしているため,反応性が大きい.
出典 朝倉書店栄養・生化学辞典について 情報