翻訳|base
精選版 日本国語大辞典 「塩基」の意味・読み・例文・類語
えん‐き【塩基】
出典 精選版 日本国語大辞典精選版 日本国語大辞典について 情報
日本大百科全書(ニッポニカ) 「塩基」の意味・わかりやすい解説
塩基
えんき
base
酸の性質を打ち消す性質をもつ物質。歴史的にみると、まず食塩のような塩の存在が知られ、ついで果汁や酸化物水溶液の酸が知られるようになった。塩基とは、塩の基(もと)、すなわち酸と反応して塩を与える物質である。陸生植物の灰から得られる炭酸カリウムや、海草の灰から得られる炭酸ナトリウムは、灰を意味するアラビア語kaliからアルカリalkaliとよばれたが、金属や有機物を侵す激しい化学反応性はその塩基性によるものである。アルカリと塩基はほとんど同じ意味に用いられているが、化学的性質を一般的に表現する用語としては塩基が適当である。
塩基は酸と相補的に成立する概念であり、1884年にスウェーデンのS・A・アレニウスは、水に溶けて水酸化物イオンOH-を放出する物質を塩基、水素イオンH+を放出する物質を酸と定義した。化学式中に含まれるヒドロキシ基-OHの数によって、一酸塩基、二酸塩基、……とよぶ塩基の分類法がある。水酸化ナトリウムNaOH、水酸化カリウムKOHは一酸塩基であり、水酸化カルシウムCa(OH)2、水酸化バリウムBa(OH)2は二酸塩基、水酸化アルミニウムAl(OH)3は三酸塩基である。
ヒドロキシ基をもたないピリジンC5H5NやアンモニアNH3も水に溶けて塩基性を示す。その原因は、水と反応して水酸化物イオンを放出することにある。
C5H5N+H2O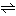 C5H5NH++OH-
C5H5NH++OH-
NH3+H2O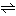 NH4++OH-
NH4++OH-
そこで1923年にデンマークのJ・N・ブレンステッドは、水に溶けて水素イオンを受け取る(結果的にOH-を放出する)物質を塩基と定義した。この定義は水以外のプロトン解離性溶媒の系にも適用できる。たとえば、液体アンモニアはきわめて小さい平衡定数ではあるが、
NH3+NH3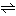 NH4++NH2-
NH4++NH2-
のような解離平衡にある。液体アンモニアに溶けてアンモニアからH+を受け取り、結果としてNH2-を放出する物質は塩基であるといえる。ブレンステッドの考えでは、塩基はつねに酸と共役関係にある。同じく1923年アメリカのG・N・ルイスは、酸と塩基に関する理論を拡張し、相手に電子対を与えて相手と共有(配位)結合をつくる物質を塩基と定義した。アレニウスおよびブレンステッドの塩基もこの定義のなかに含まれるが、配位化合物、錯体の生成反応をはじめ、多くの化学反応がルイスの酸塩基反応として説明できることになる。電子対を提供する物質、つまり電子供与体(ドナー)はルイス塩基とよばれている。三フッ化ホウ素BF3とアンモニアNH3との配位化合物生成反応、
BF3+:NH3―→F3B-NH3
を例にとると、B-N結合のための電子対を供与するアンモニアはルイス塩基であり、これを受容する三フッ化ホウ素はルイス酸である。
[岩本振武]
『水町邦彦著『酸と塩基』(2003・裳華房)』▽『山崎昶著『酸と塩基30講』(2014・朝倉書店)』
ブリタニカ国際大百科事典 小項目事典 「塩基」の意味・わかりやすい解説
塩基
えんき
base
(2) 1923年にデンマークの物理化学者 J.N.ブレンステッドは塩基と酸の定義を拡大し,プロトンを受入れることのできる物質を塩基,プロトンを与えることのできる物質を酸と定義した (→ブレンステッド=ローリーの定義 ) 。たとえば OH- イオンは,H2S+OH-→HS-+H2O のように,ほかの化合物からプロトンを受入れる力が強いので強い塩基であり,H2S は酸である。アンモニアは水溶液では NH3+H2O→NH4++OH- のようにふるまうので塩基であり,この場合,水は酸である。しかしカリウムアミド KNH2 は,液体アンモニア中で KNH2+NH3→KNH3++NH2- のように反応するので,この場合にはアンモニアは酸であり,カリウムアミドが塩基である。このようにブレンステッドの定義は非水溶媒系にも適用され,相手次第で同一物質を塩基とも酸ともみることができる。
(3) 1923年に G.N.ルイスは電子の授受に基づいて酸,塩基の定義をさらに拡張し,分子またはイオンを構成している原子の電子対により,相手と共有結合を形成できるものを塩基 (ルイス塩基 ) ,そのような電子対を受けて共有結合をつくるものを酸 (ルイス酸 ) と定義した。たとえば H3N:+BF3→H3N:BF3 の反応で,H3N: は塩基,BF3 は酸となる。このルイスの定義による塩基,酸は,ブレンステッドの定義による塩基,酸を含むと同時に OH- や H+ をもたない塩基や酸も含むので,非常に有用である。
(4) 生化学では,広く有機塩基全体をさす。アミノ基,イミノ基,グアニジル基は,上の定義からも塩基性であるから,一級アミノ基をもつセロトニン,ノルアドレナリン,二級アミノ基をもつアドレナリン,四級アミノ基をもつカルニチンはすべて塩基性物質である。また,多くの植物アルカロイド (ニコチン,モルヒン,アトロピン,エフェドリン) やポリアミン類 (スペルミン,スペルミジン) も塩基性物質である。
(5) このほか窒素を含む複素環式化合物 (ピリジン,イミダゾール,インドールなど) も塩基と呼ばれる。 DNAや RNAの構成要素であるプリン塩基 (アデニン,グアニン) とピリミジン塩基 (シトシン,チミン,ウラシル) はこの意味で用いられている。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
化学辞典 第2版 「塩基」の解説
塩基
エンキ
base
【Ⅰ】歴史的には,水溶液中で水酸化物イオンOH-を陰イオンとして放出する化合物をいう(アレニウス塩基,酸塩基の理論).その水溶液は塩基性を示す.水酸化ナトリウムNaOH,水酸化カリウムKOH,水酸化カルシウムCa(OH)2などが代表的である.近年の定義(ブレンステッド塩基)では,水素イオン H+(陽子)を受容することのできる分子またはイオン(陽子受容体).反応,
NH3 + H2O → NH4+ + OH-
ではアンモニアNH3,反応,
HCl + H2O → H3O+ + Cl-
では水H2Oが塩基である.さらに拡張されて水溶液以外でも使えるルイスの定義(ルイス塩基)では,電子対をほかの化合物に供与することのできる分子またはイオンである(電子対供与体).この定義に従えば,非共有電子対をもつ分子またはイオンが塩基で,水,アンモニアばかりでなく,アミン,ピリジン,O2-,NCS-,NO2-なども塩基である.【Ⅱ】DNAやRNAなどの核酸の塩基部分を構成する複素環.プリン環を有するアデニンとグアニンおよびピリミジン環を有するシトシン,チミン,ウラシルがある.[別用語参照]核酸,塩基対
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
知恵蔵 「塩基」の解説
出典 (株)朝日新聞出版発行「知恵蔵」知恵蔵について 情報
百科事典マイペディア 「塩基」の意味・わかりやすい解説
出典 株式会社平凡社百科事典マイペディアについて 情報
栄養・生化学辞典 「塩基」の解説
塩基
改訂新版 世界大百科事典 「塩基」の意味・わかりやすい解説
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
世界大百科事典(旧版)内の塩基の言及
【酸・塩基】より
…酸と塩基の概念には幾多の歴史的な変遷があるが,基本的には水溶液中で水素イオンを増大させるものが酸で,水素イオンを減少させるものが塩基である,とすることができる。現在の考え方からすれば,酸や塩基というべきものはかなりの数が古くから知られていたが,酸や塩基という語や概念がふつうに用いられるようになるのは17世紀ないし18世紀ころからである。…
※「塩基」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
お知らせ
4/12 日本大百科全書(ニッポニカ)を更新
4/12 デジタル大辞泉を更新
4/12 デジタル大辞泉プラスを更新
3/11 日本大百科全書(ニッポニカ)を更新
2/13 日本大百科全書(ニッポニカ)を更新
