スズ(錫) (すず)
tin
周期表第ⅣB族に属する金属元素の一つ。安定同位体の数では全元素中最も多く,112Snから124Snまで10種があり,また放射性同位体としては108Snから129Snにわたり約20種(準安定状態も含む)が知られている。天然にはスズ石SnO2として産するほか,黄錫鉱(おうしやくこう)Cu2FeSnS4としても産出する。スズは最も古くから知られていた金属の一つで,石器時代につづく時代に銅との合金である青銅として使われていたが,古くからよく知られている金属のわりには産出量が少なく,産出地も限られている。
性質
αスズ(灰色スズ,ダイヤモンド型構造,低温で安定)とβスズ(白色スズ,正方晶系,高温で安定)の二つの変態がある。転移温度は18℃であるが,この温度では転移速度が小さく,普通はβスズとして存在している。これは,不純物として微量に存在するビスマス,アンチモンなどが抑制作用をするためである。低温では転移速度が増加し,-48℃で極大となる。βスズがαスズに転移するときには膨張してくずれやすくなる。寒地で冬季にスズ器の一部がふくれて粉状になりはじめ,各部に伝わってくずれることがある。この現象は19世紀にロシアの寒冷地の博物館の展示品で見つけられ,スズペストあるいはスズの博物館病などと呼ばれた。161℃と融点との間の領域でγスズと呼ばれる変態があるといわれているが,まだ十分確認されていない。βスズは青みを帯びた白色の金属光沢をもち,100℃で著しく柔軟になるが,200℃ではかえってもろくなる。線膨張率は0℃で1.99×10⁻5deg⁻1,100℃で2.38×10⁻5deg⁻1,熱膨張に異方性がある。比抵抗は0℃で11.0μΩ・cm,100℃で15.5μΩ・cm。展性,延性に富み,加工性がよく,管にも箔にもなる。無害なので古くから食器などに広く用いられている。棒状または板状のものを曲げるとピチピチ音がする。これをスズ鳴りtin cryなどと呼ぶことがある。空気中では安定であるが,高温では燃えて酸化スズ(Ⅳ)となる。ハロゲンとは激しく作用してハロゲン化物を生ずる。両性物質で,酸に溶けて水素を発生しスズ(Ⅱ)イオンSn2⁺となるが,強アルカリにも溶けて亜スズ酸イオンSnO32⁻となる。濃硝酸には不溶性のβスズ酸をつくる。メタスズ酸と呼ぶことがあるが,正しくない。
製法
製錬用の鉱石はスズ石が主で,鉱脈から採取される山スズと,鉱脈が風化された砂スズの形が原料とされる。いずれも採鉱後,選鉱してSn60~70%程度の精鉱とする。スズ石は比重(約7)が大きいので,比重選鉱によって他の鉱物と分離される。反射炉,電気炉または溶鉱炉で,高温で炭素(コークス,無煙炭など)を用いて還元し,粗スズとする。これに含まれる不純物はおもに銅,鉛,アンチモン,ビスマス,鉄,ヒ素である。スズの鉱石にはタングステンを鉄重石FeWO4または灰重石CaWO4として,数%随伴することがある。この場合には,炭素で還元する前に,ソーダ灰(炭酸ナトリウムNa2CO3)とともに鉱石を加熱し,タングステンを水に溶けやすいタングステン酸ナトリウムNa2WO4に変え,水でタングステンを浸出分離する。
鉱石を還元する際に生ずるスラグには,なおスズを10~25%も含むので,このスラグからさらにスズを還元回収する工程がとられている。このときに得られるスズは鉄を20~30%含みハードヘッドと呼ばれる。鉄を除去して粗スズとし,鉱石から還元して得られる粗スズとともに精製される。精製には乾式法と湿式法がある。一般には,溶離法で鉄を分離し,あと電解精製する。電解液はヘキサフルオロケイ酸H2[SiF6]が用いられる。
用途
食器類,スズ箔(包装用)などのほか,ブリキ(融解したスズに鉄板を浸して表面を被覆したもの),青銅,砲金,活字合金,はんだなど各種の合金原料として用いられる。有機スズ化合物としてビニル合成の安定剤,殺菌剤,防腐剤などの原料としての用途が開発されている。
執筆者:大瀧 仁志+後藤 佐吉
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
スズ
すず
tin
周期表第14族に属し、炭素族元素の一つ。
スズはもっとも古くから知られた金属の一つで、紀元前数千年のころから地中海沿岸諸国、ペルシア、インド、中国などで広く知られていた。また少なくとも銅との合金の青銅として石器時代に続く時代に使用され、いわゆる青銅器時代を画している。ペルーのインカ遺跡からは銅に加えるための純粋なスズがみいだされている。スズという名称の起源は明らかでないが、中国では周代の紀元前1000年ごろ、すでに錫(すず)という文字が使われ、スズ冶金(やきん)、青銅などが詳しく記されている。日本では古代の青銅器製品はほとんどが中国、朝鮮からの輸入品であったし、スズそのものが知られていたわけではない。しかしスズそのものについては、8世紀ごろの記載があり、白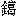 (しろめ)、白鑞(しろめ)、白﨟(ろう)などとよんでいた。宇田川榕菴(うだがわようあん)の『舎密開宗(せいみかいそう)』(1837)には「斯丹紐母(スタンニユム)、錫」と記されている。ラテン語のstannumの名称は初めはスズを意味したものではなく、銀と鉛との合金に対して用いられたが、4世紀になってスズをさすようになった。元素記号はこの語からきている。
(しろめ)、白鑞(しろめ)、白﨟(ろう)などとよんでいた。宇田川榕菴(うだがわようあん)の『舎密開宗(せいみかいそう)』(1837)には「斯丹紐母(スタンニユム)、錫」と記されている。ラテン語のstannumの名称は初めはスズを意味したものではなく、銀と鉛との合金に対して用いられたが、4世紀になってスズをさすようになった。元素記号はこの語からきている。
[守永健一・中原勝儼]
天然に錫石SnO2として産する。鉱石を炭素、珪石(けいせき)、石灰石などを加えて電気炉内で溶錬して金属とする。不純物の鉄が含まれるので、さらに還元剤などを加えて電気炉で溶錬を繰り返して粗スズを得る。これを乾式法または電解法で精錬する。このほかにブリキスズから回収される。ブリキスズを陽極として水酸化ナトリウム溶液中で電解する方法や、加圧した塩素ガスによってスズのみを塩化物とする塩素法などがある。
2011年の世界のスズの鉱石生産量は約30万1000トンで、主要国は中国(約42.2%)、インドネシア(約25.9%)、ペルー(約9.6%)である。また電気スズの生産量は約36万7000トンで、アジア(約82.6%)、北南米(約14.2%)、ヨーロッパ(約3.0%)、消費量は約38万3000トンで、アジア(約69.7%)、ヨーロッパ(約17.8%)北南米(約12.3%)となっている(WBMS:世界金属統計局)。
[守永健一・中原勝儼]
α(アルファ)-スズ、β(ベータ)-スズの2変態があり、低温で安定なのはα型で、18℃以上でβ型が安定になる。普通白色で、金属光沢があるのがβ-スズで、白色スズともよばれる。これを零下30℃以下に長時間保つとα-スズ(灰色スズという)になる。このとき金属状スズは表面に突起を生じ、ついには粉状に壊れてしまう。この現象は19世紀にロシアの博物館のスズ製品でみつけられ、スズペストとよばれた。通常は銀白色の金属で展性、延性に富み、箔(はく)や線に加工することができる。金属スズを曲げるときパチパチと音を発するが、これはティンクライTin Cry(錫鳴り)といわれている。
スズは空気中で安定であるが、熱すると燃えて酸化スズ(Ⅳ)となる。ハロゲンとは激しく反応して四ハロゲン化物を生じる。酸には水素を発して溶け、スズ(Ⅱ)塩となるが、濃硝酸ではスズ酸(酸化スズ(Ⅳ)の水和物)SnO2・nH2Oをつくる。水酸化アルカリ溶液に溶けて亜スズ酸塩をつくる。
[守永健一・中原勝儼]
スズは無害で耐食性に優れ、空気中で変色せず、外観が美しいので、鉄、鉄鋼、銅などの表面にめっきする。とくに鉄板の表面にめっきしたものをブリキという。スズめっきの対象は食器、美術工芸品から電子部品まで広い範囲にわたる。また、はんだ、青銅、減摩合金、易融合金など合金としての用途が広い。酸化物は窯業用顔料、うわぐすり(釉)、研摩剤などに、有機スズ化合物はポリ塩化ビニルの安定剤、農業用殺菌剤、重合触媒などに用いられる。
[守永健一・中原勝儼]
出典 小学館 日本大百科全書(ニッポニカ)日本大百科全書(ニッポニカ)について 情報 | 凡例
スズ
スズ
tin
Sn.原子番号50の元素.電子配置[Kr]4d105s25p2の周期表14族金属元素.原子量118.710(7).天然には質量数112~124の10種の安定同位体があり,おもなものは116(14.54(9)%),118(24.22(9)%),120(32.58(9)%).ほかに99~137の放射性同位体がある.安定同位体数のもっとも多い元素である.スズとその合金は先史時代から用いられていた金属で,元素記号Snはラテン語名stannumに由来する.本来銀と鉛の合金を意味していたが,のちにスズをさすようになった.
天然にはおもにスズ石SnO2,黄錫鉱Cu2FeSnS4として産出する.地殻中の存在度2.5 ppm.可採埋蔵量6100百万t(Sn含有量)の順位は,中国28%,マレーシア16%,インドネシア13%,ペルー12%,以下ブラジル,ボリビアである.スズ石をばい焼して,As,Sなどの不純物を除き,コークス,石灰石を加えて,高炉または反射炉で加熱還元し粗スズとする.粗スズをさらに反射炉による溶錬または電解精錬によって精製する.αスズ(灰色スズ,低温相,立方晶系)とβスズ(白色スズ,高温相,正方晶系)の2変態があり,転移温度は13.2 ℃.融解物からはβスズが結晶する.白色金属光沢のある展延性に富む金属で,密度5.75 g cm-3(20 ℃,α),7.31 g cm-3(20 ℃,β).融点231.97 ℃,沸点2270 ℃.融解熱7.194 kJ mol-1,蒸発熱290.4 kJ mol-1.第一イオン化エネルギー7.344 eV.スズの酸化数は2,4で,SnⅡは不安定で強い還元性を示す.標準電極電位(Sn2+/Sn)-0.1375 V,(Sn4+/Sn2+)+0.15 V.濃塩酸には水素を発生しながら溶けてSnⅡ Cl2に,濃硝酸では不溶性のSnO2・nH2Oになる.強アルカリと煮沸するとスズ酸塩MⅠ2[SnⅣ (OH)6]をつくって溶ける.スズは常温の空気中で安定であるが,加熱するとSnⅣ O2を生じる.フッ素以外のハロゲンXとはげしく反応して,SnⅣ X4を生じる.室温ではフッ素に対して安定であるが,高温ではSnF2,SnF4をつくる.[SnIⅡCl3]-,[SnIⅡCl4]2-,[SnIⅡBr3]- のようなハロゲノ錯イオンや,[Sn(C2O4)2]2-,[SnⅣ(OH)6]2- なども知られている.スズは水素よりイオン化傾向が大きく,Ag,Hg,Bi,Cu,Pt,Auなどのイオンを金属まで還元することができる.また,多くの有機スズ化合物が知られている.
用途は,スズめっき([別用語参照]ブリキ),缶用スズめっき鋼板,スズはくの製造のほか,多くの金属と合金をつくりやすいことから青銅,はんだ,軸受合金,活字合金などの原料として広く使われている.酸化スズインジウム(ITO)はフラットパネルディスプレイ用透明電極として需要が増加している.リン青銅(Cu-Sn-P)は電子部品リードフレームに使われる.有機スズ化合物はプラスチック安定剤,防かび剤などに使用される.わが国の最大の用途は,スズを主成分とするはんだ用で約30%,ついで有機スズ化合物など化成品15% 強,スズめっき缶・鋼板用約15% 弱,電子部品用10% 弱で,透明電極用の使用量は1~2% とされる.消費量約35000 t のほぼ全量をインドネシア,中国,マレーシアからの輸入と鉱さい,煙灰などからのリサイクル(~750 t)でまかなった(2005年)[CAS 7440-31-5]
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
スズ
tin
元素記号 Sn ,原子番号 50,原子量 118.710。周期表 14族,炭素族元素の1つ。最も古くから知られていた金属元素の1つで,天然にはスズ石として産し,これがほとんど唯一の鉱石である。地殻存在量2~3ppm,海水中の存在量1 μg/l 。単体は銀白色の展延性に富む金属で,比重 7.28,融点 232℃。粉末にしやすい。 200℃に加熱すると,もろい斜方スズとなる。空気中や水中で安定,希酸に溶けにくいが,濃塩酸,王水と反応して溶ける。アルカリ溶液とも反応して溶ける。ブリキ製造に多量に用いられるほか,青銅,はんだ,ブリタニヤ合金,種々の軸受合金の製造に使用される。化合物としても染色工業などに多くの用途がある。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
スズ
原子番号50,原子量118.70,元素記号Sn,14族(旧IVa族)の元素.必須微量元素.
出典 朝倉書店栄養・生化学辞典について 情報
世界大百科事典(旧版)内のスズの言及
【海峡植民地】より
…海峡植民地を含めたこれらをイギリス領マラヤと総称した。 海峡植民地はマレー半島のゴム,スズの輸出に基礎を置くばかりでなく,中継貿易基地として繁栄した。なかでもシンガポールが重要であった。…
【海峡スズ(海峡錫)】より
…マレー半島で産出するスズの総称。第2次大戦後,この言葉はあまり用いられなくなった。…
【非鉄金属鉱業】より
…非鉄鉱物資源を探査・発見し,これを採掘・取得し,選鉱・製錬する産業。非鉄金属とは広義には鉄以外の金属すべてのことであるが,一般的には銅,鉛,亜鉛,スズ,ニッケル,コバルト,タングステンなどのことを指し,[金],[銀]などは貴金属,アルミニウム,マグネシウム,チタンは軽金属として区別されることが多い。世界の生産量(含有量)は銅鉱1002万tで,うちチリ249万t,アメリカ185万t,旧ソ連80万tなど,鉛鉱は269万tで,うちオーストラリア45万t,アメリカ41万t,中国40万tなど,亜鉛鉱は700万tで,うちカナダ111万t,中国100万t,オーストラリア90万tなど,スズ鉱は19万4600tで,うち中国5万4000t,インドネシア4万6100t,ペルー2万2300tなどである(1995)。…
【ボリビア】より
…1人当り国民総生産は770ドル(1994)で,かつ所得格差が大きく,工業化の進展の度合は低い。 ボリビアの経済構造は基本的には鉱産物(とくにスズ)の輸出を中心としたモノカルチャー経済であったが,近年鉱産物の比重が低下し,一次産品開発の多角化が進んだ。輸出のうち,鉱産物が40%,近年開発された石油・天然ガスが25%を占めるほか,大豆,木材,宝飾品など非伝統産品の割合が増加している(1990)。…
【木星】より
…【田中 済】
[シンボリズム]
木星は最大の惑星であり,ギリシア・ローマ神話の神々の王たる[ゼウス],[ユピテル](英語のジュピター)と同一視された。錬金術ではスズのシンボル。占星術では大いなる幸福の惑星とみなされ,吉位にある場合は長寿と栄誉をもたらし,率直,博愛,賢明,正義の性質を授けるとされる。…
※「スズ」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」


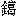 (しろめ)、白鑞(しろめ)、白﨟(ろう)などとよんでいた。宇田川榕菴(うだがわようあん)の『舎密開宗(せいみかいそう)』(1837)には「斯丹紐母(スタンニユム)、錫」と記されている。ラテン語のstannumの名称は初めはスズを意味したものではなく、銀と鉛との合金に対して用いられたが、4世紀になってスズをさすようになった。元素記号はこの語からきている。
(しろめ)、白鑞(しろめ)、白﨟(ろう)などとよんでいた。宇田川榕菴(うだがわようあん)の『舎密開宗(せいみかいそう)』(1837)には「斯丹紐母(スタンニユム)、錫」と記されている。ラテン語のstannumの名称は初めはスズを意味したものではなく、銀と鉛との合金に対して用いられたが、4世紀になってスズをさすようになった。元素記号はこの語からきている。